Используя свет вместо тепла, исследователи из Национальной лаборатории Ок-Риджа Министерства энергетики нашли новый способ выделения углекислого газа (CO2) из растворителя, используемого при прямом улавливании воздуха, или DAC, для улавливания этого парникового газа. Новый подход прокладывает путь к экономически целесообразному выделению CO2 из атмосферы.
Выделение углекислого газа по требованию возможно благодаря тому, что долгоживущее возбужденное состояние новой кислоты контролирует концентрацию протонов в растворе с помощью ультрафиолетового излучения, создавая условия, которые приводят к энергоэффективному выделению CO2. Напротив, современные технологии DAC фильтруют воздух через водный раствор, содержащий сорбирующий материал, такой как аминокислота, который поглощает атмосферный CO2 и удерживает его. Нагрев растворителя высвобождает CO2 и регенерирует аминокислоту для вторичной переработки. CO2 может быть либо сохранен, либо преобразован в продукты с добавленной стоимостью, такие как этанол, полимеры или бетон.
“В существующих технологиях прямого улавливания воздуха выделение CO2 и регенерация сорбента являются наиболее энергоемкими этапами”, – сказал химик ORNL Инчжонг Ма, возглавлявший исследование, опубликованное в международном издании Angewandte Chemie, совместно с коллегами из ORNL Раду Кустельчаном и Увиндуни Премадасой, химиками. “Цель здесь состоит в том, чтобы использовать аминокислотный сорбент, который пригоден для вторичной переработки и обладает множеством привлекательных свойств, в сочетании с более энергоэффективным подходом к выделению CO2 и регенерации сорбента”.
Национальная академия наук пришла к выводу, что технологии DAC играют определенную роль в ежегодном удалении миллиардов тонн CO2 из атмосферы, помогая ограничить повышение средней глобальной температуры менее чем на 2 градуса по Цельсию (около 4 градусов по Фаренгейту). Однако высокие энергозатраты, связанные с регенерацией сорбента и выделением CO2 в масштабах, которые позволили бы смягчить последствия изменения климата, превращают такое массовое внедрение в серьезную проблему, требующую разработки новых процессов DAC. Подход, основанный на ORNL, обеспечил подтверждение концепции использования облучения ультрафиолетовым светом в условиях окружающей среды вместо нагревания раствора для выделения CO2 и регенерации сорбента.
“Нагрев водных растворов – распространенный метод регенерации, но он чрезвычайно энергоемкий”, – сказал Кустелсеан, пионер в области DAC. “Мы хотели исключить тепло из уравнения”.
В 2017 году Кастельс провел исследование, которое доказало, что гуанидиновый сорбент может непосредственно улавливать CO2 из воздуха. В 2018 году он и его коллеги продемонстрировали практичный, энергоэффективный метод DAC, использующий солнечное тепло для стимулирования выделения парниковых газов из аминокислотного сорбента. В этом году стартап Holocene из Ноксвилла лицензировал технологию, чтобы подготовить ее к промышленному внедрению.
В этой новой разработке ключом к выделению CO2 в условиях окружающей среды является фотокислота, представляющая собой молекулу, которая становится более кислой, когда поглощает свет. Посветите на кислоту, такую как уксус, и ничего не произойдет. Напротив, подвергните фотокислоту воздействию ультрафиолетового или видимого света, и химическая группа в середине кислоты повернется с противоположной стороны связи на ту же сторону. Последующая реакция образует кольцо, приводящее к переносу протона или иона водорода в водный растворитель.
Этот перенос резко повышает кислотность раствора, вызывая изменение, называемое “колебанием рН”. Избыток протонов теперь может взаимодействовать с бикарбонатом, или HCO3–, который образуется при взаимодействии CO2 с сорбентом. Бикарбонат принимает протон, превращаясь в углекислоту, или H2CO3, которая находится всего в одном энергетически выгодном шаге от углекислого газа и воды.
“В этой статье впервые описан случай, когда макроскопическое изменение рН, длящееся от минут до часов, было продемонстрировано с использованием света в качестве внешнего триггера для инициирования реакции регенерации CO2”, – сказал Вячеслав “Слава” Брянцев, руководитель группы химического разделения ORNL и соавтор статьи.
“Вы можете легко включать и выключать свет, чтобы обратимо контролировать реакцию”, – сказала Ма. “Вы можете улавливать CO2 в темноте, а затем просто включать свет, когда хотите высвободить CO2 для хранения или производства продуктов с добавленной стоимостью. Это дает вам возможность легко контролировать процесс по требованию”.
Тем не менее, исследователям требовался дополнительный трюк со светом. Обычные фотокислоты не сработали бы, потому что время жизни их возбужденных состояний очень короткое — всего лишь наносекунды. Они теряют протоны, но затем остаются в основном в той же конфигурации. “Тогда вы меняете кислотность только на короткое время”, – сказал Брянцев.
Ма и Кустелсеан, которым пришла в голову идея использовать фотокислоту для запуска выделения CO2 в приложениях DAC, столкнулись с этой проблемой, когда начали эксперименты с использованием коммерчески доступной фотокислоты.
Используя свет вместо тепла, исследователи из Национальной лаборатории Ок-Риджа Министерства энергетики нашли новый способ выделения углекислого газа, или CO2, из растворителя, используемого при прямом улавливании воздуха, или DAC, для улавливания этого парникового газа. Новый подход прокладывает путь к экономически целесообразному выделению CO2 из атмосферы.
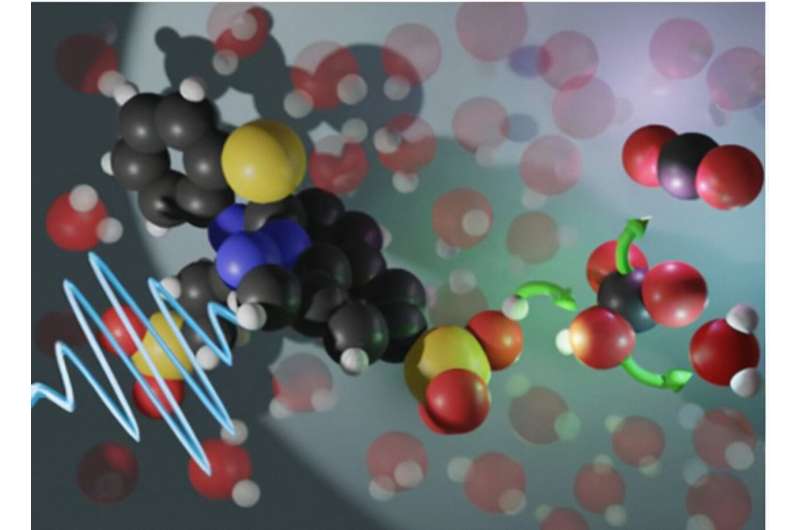
Аминокислотные сорбенты, содержащиеся в воде, могут улавливать углекислый газ (CO2) непосредственно из воздуха. Аминогруппа вступает в реакцию с CO2 с образованием смеси химических веществ, включая бикарбонат (HCO3-). Исследователи добавили в эту смесь фотокислоту (PA). Когда реакционная камера подвергалась воздействию света, фотокислота претерпевала структурные изменения и переносила протон в воду. Эти события делают смесь более кислой и смещают ее баланс в сторону образования большего количества углекислоты (H2CO3), которая нестабильна и при комнатной температуре легко превращается в CO2 и воду. Когда реакционная камера закрывается для блокирования света, фотокислота возвращается к своей первоначальной протонированной форме (транс-конфигурация), и аминокислоты теперь готовы (депротонированы) для следующего цикла улавливания CO2.
“Когда углекислота разлагается, ее срок службы в воде невелик, порядка нескольких секунд. Но это бесконечность по сравнению со временем жизни обычной фотокислоты, которое составляет наносекунды, или миллиардные доли секунды”, – сказал Кустелчан. “Вот почему вы не можете провести эту химию с обычной фотокислотой: для выделения CO2 из углекислоты требуются секунды, но фотокислоте требуется всего наносекунды, чтобы вернуть протон обратно”.
Брянцеву пришла в голову идея попробовать другой класс фотокислот с долгоживущим возбужденным состоянием. Называемая фотокислотой в метастабильном состоянии, она имеет структуру, которая сохраняется в растворе от секунд до часов. Это означает, что изменение рН, вызванное структурными изменениями фотокислоты, также длится намного дольше.
Ученые пригласили эксперта по разработке и синтезу фотокислот присоединиться к команде. Йи Ляо из Флоридского технологического института стал пионером нового класса фотокислот в метастабильном состоянии примерно в 2015 году, но для других целей, кроме DAC.
“Мы действительно совершили прорыв после того, как получили эту фотокислоту от нашего сотрудника”, – сказала Ма.
Кустелсан согласился. “Наличие фотокислоты в метастабильном состоянии дало нам достаточно времени для высвобождения протона и образования углекислоты. Затем углекислота успела выделить CO2 в воде. Как только это происходит, CO2 покидает раствор”, – сказал он.
Совместно с Ма, первым автором Премадаса разработал и провел эксперименты для проверки концепции с использованием фотокислоты в метастабильном состоянии, синтезированной Ляо и его коллегой из Флоридского технологического института Аднаном Элгаттаром, с последующей спектроскопической характеристикой Бенджамином Даути и Верой Бочаровой из ORNL.
“Как только мы определили фотохимические свойства самой кислоты, нашим следующим шагом было проверить ее применимость для выделения CO2 с помощью различных сорбентов DAC”, – сказал Премадаса. “Мы можем легко манипулировать химическим составом, интенсивностью и цветами света, чтобы стимулировать фотореакцию для эффективного выделения CO2”.
Одри Майлз из Университета Нотр-Дам и Стелла Белони из Университета Флориды, которые на момент проведения исследования проходили стажировку в лаборатории бакалавриата наук Министерства энергетики США, протестировали фотокислоту в различных условиях на предмет ее способности выделять CO2. Затем Мишель Киддер из ORNL, Диана Стамберга и Джошуа Дамрон измерили количество CO2, выделяющегося при этих различных условиях.
Остается много проблем, связанных с разработкой технологии ЦАП ORNL, активируемой светом. Одним из них является понимание динамики, посредством которой фотокислота образует химический комплекс с аминокислотным сорбентом. Другой способ – улучшение растворимости соединений в воде. Еще одним способом является оптимизация поглощения света из видимого спектра. Более того, ученые хотели бы сократить время, необходимое для регенерации фотокислоты, и улучшить понимание ее долгосрочной стабильности.
Как бы то ни было, будущее за фотокислотами в метастабильном состоянии светлое. “Наше исследование прокладывает путь к фотохимическим подходам к выделению CO2 и регенерации сорбента с использованием солнечного света”, – сказал Премадаса.
Статья называется “Фотохимически управляемое выделение CO2 с использованием фотокислоты в метастабильном состоянии для энергоэффективного прямого улавливания воздуха”.